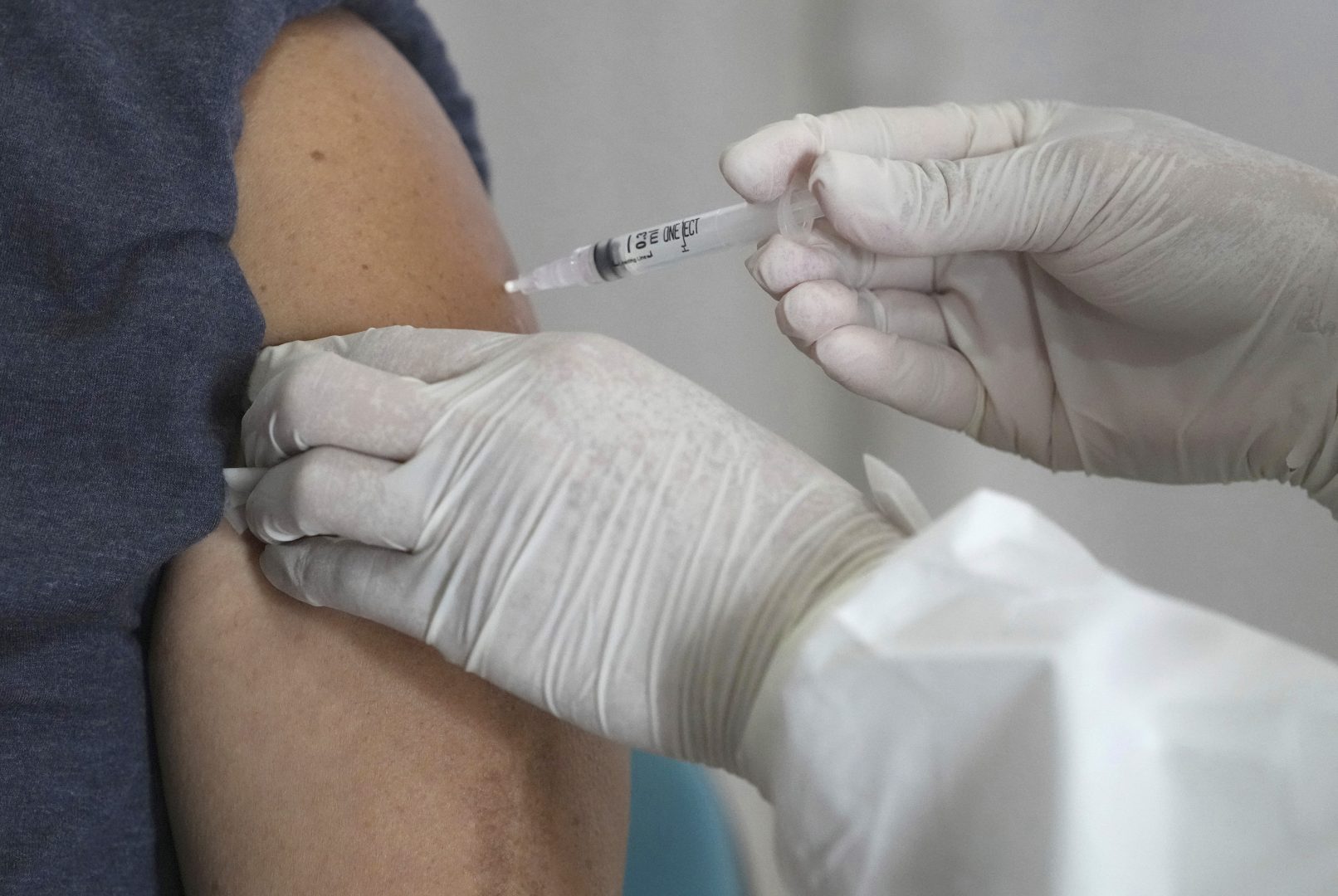
Администрацията на САЩ за храните и лекарствата (FDA) даде одобрението си за прилагане на бустерна доза от ваксината на Pfizer-BioNTech слещу коронавирус при деца на възраст от 5 до 11 години. В изявлението на агенцията е подчертано, че децата в тази възрастова група могат да получа бустера най-рано 5 месеца след стандартната ваксинация от две инжекции. Бустерната доза е от 10 микрограма - същата като при стандартната ваксинация за тази група и една трета от дозата, давана на хора над 12 години. Решението но FDA сега отива в CDC, където ще направят препоръки за начина на употреба. ТЕхният независим панел от експерти, Advisory Committee on Immunization Practices, ще обсъди бустерната доза на среща, насрочена за четвъртък. Очаква се след съвещанието директорът на CDC д-р Рошел Уаленски да издаде финалните препоръки.