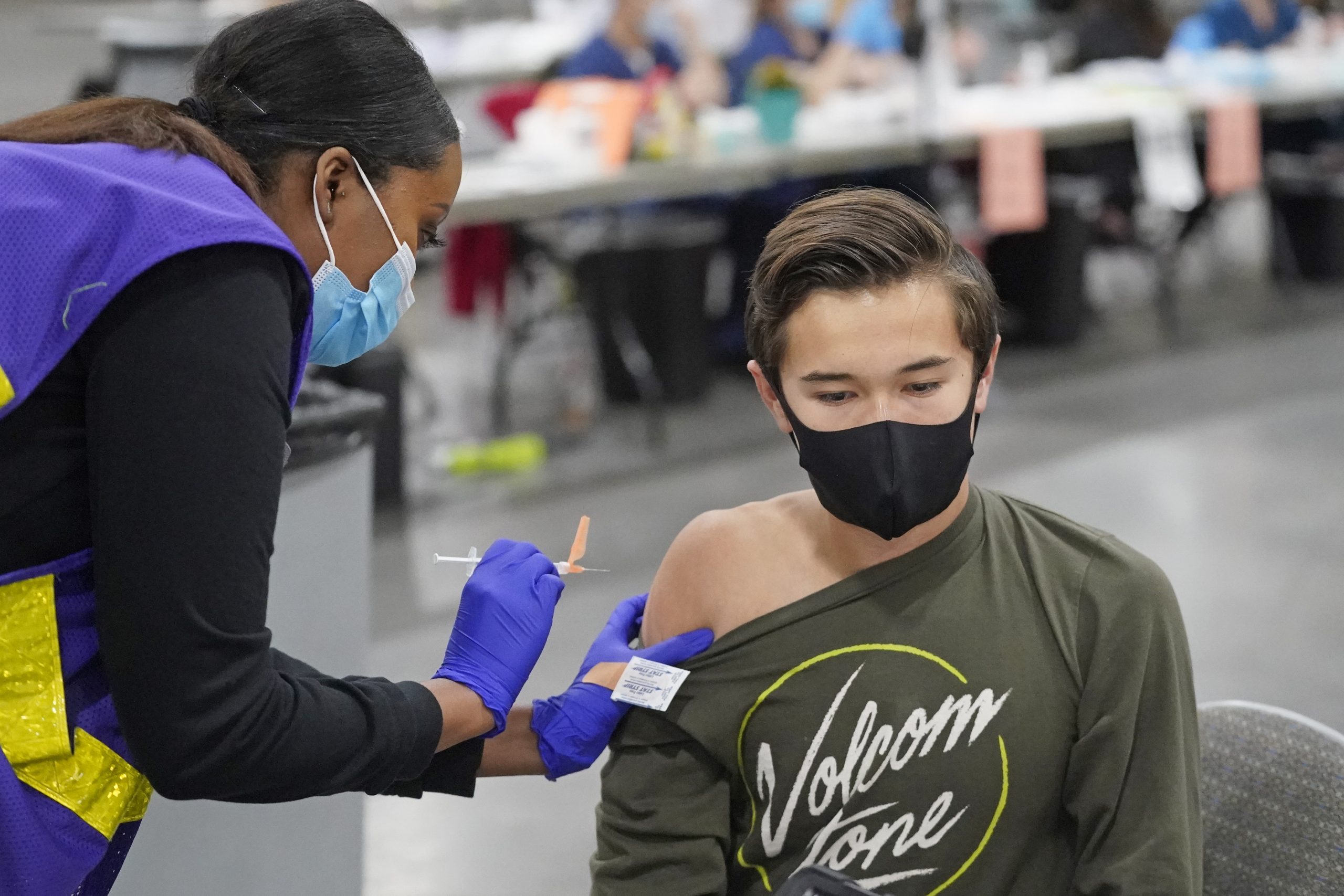
"Pfizer" и "BioNTech" започнаха тестове на ваксината си срещу COVID-19 при деца под 12 г. с надеждата за разширяване на имунизацията сред тази възрастова група към началото на следващата година.
Първите доброволци в ранния етап на изследването са ваксинирани в сряда, каза говорителката на "Pfizer" Шарън Кастийо.
Ваксината срещу COVID-19 на "Pfizer"/"BioNTech" получи разрешение от регулаторните власти в САЩ в края на декември за приложение при лица на и над 16-годишна възраст. Близо 66 милиона дози от нея са приложени в САЩ до сряда сутринта, сочат данни на американските Центрове за контрол и профилактика на заболяванията.
Педиатричното изследване, в което ще участват и деца на 6 месеца, започва седмица след началото на подобни тестове на "Moderna".
Само ваксината на "Pfizer"/"BioNTech" се използва при 16-годишни и 17-годишни лица в САЩ. Препаратът на "Moderna" получи одобрение за приложение при навършили 18 години. Досега няма ваксина, която да е одобрена за използване при деца.
"Pfizer" и "BioNTech" възнамеряват първоначално да изпробват безопасността на двудозова ваксина при три различни дозировки - от 10, 20 и 30 микрограма сред 144-ма участници в първа и втора фаза на клиничните тестове.
В третата фаза се предвижда да участват 4500 души, върху които ще се провери безопасността, поносимостта и имунният отговор в резултат на ваксината чрез измерване на нивата на антитела при децата.
Говорителката съобщи, че двете компании се надяват да разполагат с данни от изследването през втората половина на 2021 г.
Междувременно "Pfizer" изпробва ваксината сред деца на възраст 12-15 години. Компанията очаква резултати от това изследване в следващите седмици, каза Кастийо.
Помогни BG VOICE да излиза на хартия
Подкрепете независимата журналистика! Вашите дарения ни помагат да продължаваме да ви предоставяме актуални, проверени и значими новини.